|
Multizentrische, randomizierte placebo-kontrollierte klinische Prüfung (Phase III)
EudraCT 2022-001682-12 NCT05619653 |
Randomisierte, placebo-kontrollierte klinische Prüfung der Wirksamkeit des myokardialen Schutzes bei Patienten mit postakuter entzündlicher Herzbeteiligung infolge COVID-19 Infektion |
|
Am Institut für Experimentelle und Translationale Kardiovaskuläre Bildgebung führen wir eine randomisierte, placebokontrollierte klinische Studie zur kardioprotektiven Behandlung (MYOFLAME-19) bei zuvor gesunden Personen mit langer COVID-Infektion und kürzlich erfolgter COVID-Infektion und Herzbeschwerden (Kurzatmigkeit bei Anstrengung, Brustschmerzen, Tachykardie) durch. Die aktive Rekrutierung von Patienten erfolgt an 3 deutschen Standorten (Greifswald, Frankfurt, Kiel) und 1 österreichischen Standort (Wien).
Wenn Sie an einer Teilnahme interessiert sind, melden Sie sich bitte über die Website der Studie an. In klinischen Studien testen wir ein bestehendes oder neues Medikament in einer randomisierten, doppelblinden (placebokontrollierten) Studie. Wir versuchen herauszufinden, ob die Behandlung zu einer Verbesserung führt. In der Myoflame-19-Studie wird die Wirkung der Behandlung durch Messungen am Herzen (16 Wochen) und durch verbesserte Ergebnisse (1- und 5-Jahres-Follow-up) bewertet. Doppelblind bedeutet, dass einige Patienten die Behandlung erhalten und andere nicht, was aber weder der Patient noch der Arzt weiß. Alle Herzmessungen werden von einem speziellen unabhängigen Team (Core-Lab) durchgeführt. Prüfer und Teilnehmer bleiben gegenüber der Gruppenzuweisung und den Ergebnissen der Bildgebung verblindet. |
Bei Interesse an die Studie, klicken Sie hier
Überblick |
Long COVID oder postakute Folgen einer COVID-19-Infektion (PASC) sind zunehmend anerkannte Komplikationen, die sich durch anhaltende Symptome auszeichnen, die vor der Infektion nicht vorhanden waren. Herzsymptome, die auf eine postakute entzündliche Herzbeteiligung zurückzuführen sind, betreffen ein breites Spektrum von Menschen, die zuvor gesund waren und möglicherweise nur eine leichte akute Erkrankung hatten (PASC-Cardiovascular Syndrome, PASC-CVS). Die Symptome können im Zusammenhang mit der akuten Erkrankung auftreten, häufiger treten sie jedoch mit Verzögerung auf. Zu den Symptomen im Zusammenhang mit dem Herz-Kreislauf-System gehören Belastungsdyspnoe, Belastungsintoleranz, Engegefühl in der Brust, ziehende oder brennende Schmerzen in der Brust und Herzklopfen (POTS, Anstrengungstachykardie).
Pathophysiologisch steht die lange COVID im Zusammenhang mit einer Erkrankung der kleinen Gefäße (Endotheldysfunktion), einer vaskulären Dysfunktion und einer daraus resultierenden Hypoperfusion der Gewebeorgane aufgrund einer anhaltenden Dysregulation des Immunsystems. Aktive Organe mit hoher Sauerstoffabhängigkeit sind am meisten betroffen (Herz, Gehirn, Nieren, Muskeln usw.). Daher werden kardiale Symptome häufig von Manifestationen anderer Organsysteme begleitet, darunter Müdigkeit, Hirnnebel, Nierenprobleme, Myalgien, Haut- und Gelenkmanifestationen usw., die alle Teil des Long-COVID- oder PASC-Syndroms sind.
Phänotypisch ist die post-COVID-Herzbeteiligung durch chronische perivaskuläre und myoperikardiale Entzündungszeichen gekennzeichnet. Das Muster ähnelt dem, das bei chronischen systemischen Autoimmunerkrankungen beobachtet wird. Wir und andere haben Veränderungen mittels empfindlicher kardialer MRT-Bildgebung nachgewiesen und gezeigt, dass die MRT-Befunde mit kardialen Symptomen zusammenhängen.
Wir stellen die Hypothese auf, dass ein frühzeitiges Eingreifen mit Immunsuppression und Antimodellierungstherapie die Symptome und die Entwicklung von Myokardschäden verringern kann, indem die Krankheitsaktivität minimiert und eine Remission der Krankheit herbeigeführt wird. Eine niedrig dosierte Erhaltungstherapie kann dazu beitragen, die Krankheitsaktivität auf einem möglichst niedrigen Niveau zu halten. Die Vorteile einer frühzeitigen Einleitung einer Antimodellierungstherapie zur Verringerung der Symptome von Belastungsunverträglichkeiten sind allgemein anerkannt, werden aber außerhalb des klassischen kardiologischen Kontextes, wie z. B. bei Herzinsuffizienz oder Bluthochdruck, nicht häufig eingesetzt. Da die meisten Patienten mit entzündlichen Herzerkrankungen nur leichte oder keine strukturellen Anomalien haben, werden sie nicht behandelt (Standardbehandlung).
Pathophysiologisch steht die lange COVID im Zusammenhang mit einer Erkrankung der kleinen Gefäße (Endotheldysfunktion), einer vaskulären Dysfunktion und einer daraus resultierenden Hypoperfusion der Gewebeorgane aufgrund einer anhaltenden Dysregulation des Immunsystems. Aktive Organe mit hoher Sauerstoffabhängigkeit sind am meisten betroffen (Herz, Gehirn, Nieren, Muskeln usw.). Daher werden kardiale Symptome häufig von Manifestationen anderer Organsysteme begleitet, darunter Müdigkeit, Hirnnebel, Nierenprobleme, Myalgien, Haut- und Gelenkmanifestationen usw., die alle Teil des Long-COVID- oder PASC-Syndroms sind.
Phänotypisch ist die post-COVID-Herzbeteiligung durch chronische perivaskuläre und myoperikardiale Entzündungszeichen gekennzeichnet. Das Muster ähnelt dem, das bei chronischen systemischen Autoimmunerkrankungen beobachtet wird. Wir und andere haben Veränderungen mittels empfindlicher kardialer MRT-Bildgebung nachgewiesen und gezeigt, dass die MRT-Befunde mit kardialen Symptomen zusammenhängen.
Wir stellen die Hypothese auf, dass ein frühzeitiges Eingreifen mit Immunsuppression und Antimodellierungstherapie die Symptome und die Entwicklung von Myokardschäden verringern kann, indem die Krankheitsaktivität minimiert und eine Remission der Krankheit herbeigeführt wird. Eine niedrig dosierte Erhaltungstherapie kann dazu beitragen, die Krankheitsaktivität auf einem möglichst niedrigen Niveau zu halten. Die Vorteile einer frühzeitigen Einleitung einer Antimodellierungstherapie zur Verringerung der Symptome von Belastungsunverträglichkeiten sind allgemein anerkannt, werden aber außerhalb des klassischen kardiologischen Kontextes, wie z. B. bei Herzinsuffizienz oder Bluthochdruck, nicht häufig eingesetzt. Da die meisten Patienten mit entzündlichen Herzerkrankungen nur leichte oder keine strukturellen Anomalien haben, werden sie nicht behandelt (Standardbehandlung).
Ziele der Studie
Das übergeordnete Ziel ist es, zu untersuchen, ob eine frühzeitige kombinierte Immunsuppressions-/Antimodeling-Therapie bei Patienten mit PASC-CVS und Anzeichen einer subklinischen Entzündung im kardialen MRT zu einer Verringerung der Symptome und der entzündlichen Myokardschädigung sowie langfristig zu einer geringeren Entwicklung einer Herzinsuffizienz führt.
Wer nimmt teil
Personen mit dokumentierter COVID-19-Infektion, die nach der COVID-19-Infektion neue kardiale Symptome aufweisen, die die vordefinierten CMR-Kriterien für eine PostCOVID-Myokardbeteiligung erfüllen und keine zuvor bekannte oder nachweisbare strukturelle Herzerkrankung aufweisen, werden in die Studie aufgenommen. Die Teilnehmer haben zuvor keine ACE-Hemmer oder Angiotensin-Rezeptor-Blocker eingenommen. Die Teilnehmer haben innerhalb der letzten 10 Wochen keine entzündungshemmende oder immunsuppressive Behandlung oder Intervention erhalten. Die genaue Liste der Einschluss- und Ausschlusskriterien ist auf der Website clinicaltrial.gov NCT05619653 zu finden.
Wie ist der Ablauf der Studie
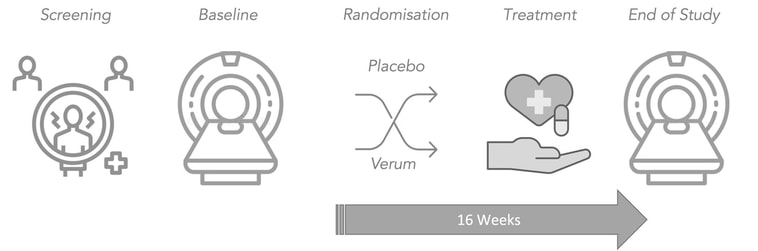
Die Teilnehmer werden zunächst gebeten, einen Screening-Fragebogen auszufüllen. Anschließend wird ein Gespräch über die Studie geführt. Wenn die Teilnehmer bereit sind, mit der Studie fortzufahren, unterzeichnen sie eine Einverständniserklärung und werden zur Erstuntersuchung eingeladen.
Bei der Erstuntersuchung wird durch eine MRT-Untersuchung des Herzens festgestellt, ob die Teilnehmer die Einschlusskriterien für die Behandlung erfüllen. Außerdem werden eine Blutentnahme und kardiopulmonale Tests durchgeführt.
Die Teilnehmer, die die Kriterien für die Herz-MRT erfüllen, werden nach dem Zufallsprinzip entweder einer Behandlung (Losartan und Prednisolon) oder einem Placebo zugeteilt. Die Teilnehmer nehmen die Behandlung bzw. das Placebo über einen Zeitraum von insgesamt 16 Wochen ein. Während der 16 Wochen werden sie engmaschig überwacht und unterstützt.
Am Ende der 16 Wochen nehmen die Teilnehmer an der Abschlussuntersuchung mit Herz-MRT, Blutentnahme und CPET teil. Die Teilnehmer werden nach Abschluss des Behandlungszeitraums sowie nach 1 und 5 Jahren weiter beobachtet. Insgesamt werden 280 Patienten in die Studie aufgenommen.
Bei der Erstuntersuchung wird durch eine MRT-Untersuchung des Herzens festgestellt, ob die Teilnehmer die Einschlusskriterien für die Behandlung erfüllen. Außerdem werden eine Blutentnahme und kardiopulmonale Tests durchgeführt.
Die Teilnehmer, die die Kriterien für die Herz-MRT erfüllen, werden nach dem Zufallsprinzip entweder einer Behandlung (Losartan und Prednisolon) oder einem Placebo zugeteilt. Die Teilnehmer nehmen die Behandlung bzw. das Placebo über einen Zeitraum von insgesamt 16 Wochen ein. Während der 16 Wochen werden sie engmaschig überwacht und unterstützt.
Am Ende der 16 Wochen nehmen die Teilnehmer an der Abschlussuntersuchung mit Herz-MRT, Blutentnahme und CPET teil. Die Teilnehmer werden nach Abschluss des Behandlungszeitraums sowie nach 1 und 5 Jahren weiter beobachtet. Insgesamt werden 280 Patienten in die Studie aufgenommen.
Was passiert mit Ergebnissen
Alle MRT-Untersuchungen des Herzens werden nach einem vordefinierten standardisierten Bildgebungsprotokoll durchgeführt. Alle Bilder werden in einem speziellen Kernlabor analysiert, um zu bestätigen, dass die Teilnehmer für die Studie in Frage kommen, und um die abschließenden Bewertungen durchzuführen. Um die wissenschaftliche Validität der Studienergebnisse zu gewährleisten, bleiben Prüfer und Teilnehmer hinsichtlich der Gruppenzuordnung und der Bildgebungsergebnisse verblindet. Die Ergebnisse werden nach Abschluss der Studie von einem unabhängigen Statistiker ausgewertet. Die Ergebnisse werden zur Veröffentlichung bei einer Fachzeitschrift mit Peer-Review eingereicht.
Organisation der Studie
Es handelt sich um eine vom Prüfarzt initiierte Forschungsstudie, die durch industrielle Mittel (Bayer AG) unterstützt wird. Die Goethe-Universität Frankfurt ist der Sponsor der Studie (Sponsorenvertreter/Hauptprüfer Dr. Valentina Puntmann und Eike Nagel). Die Durchführung der Studie wird von einem Lenkungsausschuss und einem Ausschuss für Datensicherheit und -überwachung überwacht. Die Studie wird von der Alcedis GmbH, einem Unternehmen für klinische Forschung, unterstützt und überwacht.